1. Morfología
2. Síntesis proteínas
- Control calidad
3. Síntesis de lípidos
4. Detoxificación
5. Homeostasis glucosa
6. Almacén de calcio
7. Vesículas
8. Contactos membranas
9. Peroxisomas
10. Gotas de lípidos
11. Autofagia
El retículo endoplasmático es un orgánulo delimitado por membrana que forma una compleja red de túbulos y cisternas que se extienden por todo el citoplasma celular. Posee tres dominios que son el retículo endoplasmático rugoso, el retículo endoplasmático liso y la envuelta nuclear. El retículo endoplasmático rugoso se caracteriza por tener ribosomas asociados a sus membranas y por organizarse en forma de cisternas aplanadas y túbulos. El retículo endoplasmático liso no tiene ribosomas asociados a sus membranas y se organiza en túbulos muy contornoeados. Como su nombre indica, al pensar en el retículo endoplasmático hay que verlo como un entramado reticular de túbulos y cisternas conectados entre sí. Este nombre se propuso tras ver las primeras imágenes de este orgánulo con el microscopio electrónico. Aunque la envuelta nuclear realiza funciones muy específicas relacionadas con el núcleo, puede ser considerada como el tercer dominio del retículo endoplasmático, puesto que es continua con las membranas del retículo endoplasmático rugoso. Las principales funciones de este orgánulo son la síntesis de proteínas, de lípidos, glicoconjugados, almacén de calcio y la organización del núcleo, aunque desarrolla otras funciones también críticas para la célula. Es el orgánulo más grande de la mayoría de las células y puede representar hasta la mitad del todal de las membranas de una célula animal típica.
A pesar de su tamaño, el retículo endoplasmático fue descrito con el microscopio óptico después que otros orgánulos. Fue inicialmente descrito en 1902 por A. Veratti (discípulo de Camilo Golgi), y posteriormente observado con el microscopio electrónico por V. Porter y G. Palade en los años 50 del siglo XX. V. Porter le dio el nombre de retículo endoplasmático, lo que ya indicaba su estructura intrincada.
1. Morfología
El retículo endoplasmático es un complejo sistema reticular de membranas dispuestas en forma de sacos o cisternas aplanados y túbulos que están interconectados entre sí compartiendo el mismo espacio interno. Sus membranas se extienden desde la envuelta nuclear hasta las proximidades de la membrana plasmática, llegando a representar más de la mitad de las membranas de una célula animal, y pudiendo ser hasta 10 veces más extensas que la membrana plasmática.
El retículo endoplasmático se organiza en tres dominios principales que realizan diferentes funciones. Las cisternas y los túbulos que poseen ribosomas asociados se han denominado tradicionalmente como retículo endoplasmático rugoso, mientras que los túbulo sin ribosomas asociados se agrupan como retículo endoplasmático liso (Figuras 1 y 2). La envuelta nuclear, cuya membrana se continúa con las del retículo endoplasmático rugoso y liso, es el tercer dominio del retículo, pero sus funciones se suelen estudiar en relación con la organización del núcleo y la expresión génica (ver envuelta nuclear). En las células de las plantas se reconoce un domino adicional del retículos endoplasmático: las membranas que froman el desmotúbulo en los plasmodesmos.


Las cisternas y los túbulos del retículo endoplasmático pueden ocupar espacios celulares diferentes en el citoplasma, como ocurre en los hepatocitos, en las neuronas y en las células que sintetizan esteroides. Sin embargo, en algunas regiones del citoplasma no existe una segregación clara entre ambos dominios y se aprecian áreas de membrana en forma de cisterna entremezcladas con túbulos. La disposición espacial del retículo endoplasmático en las células animales depende en gran medida de sus interacciones con los microtúbulos, mientras que en las vegetales son los filamentos de actina los principales responsables de su organización. En las células animales la generación de nuevos túbulos depende de los movimientos de tracción de las proteínas motoras sobre los microtúbulos. Así, literalmente arrastrarían a membranas de retículo endoplasmático generando un túbulo nuevo. Pero además se ha visto que un túbulo se puede asociar al extremo en polimerización de un microtúbulo y crecer ambos al unísono. Sin embargo, el citoesqueleto no parece participar en el mantenimiento de la forma de cisterna o de los túbulo una vez formados.
Cómo se organiza el retículo endoplasmático en la célula pende del tipo celular y puede cambiar según el estado fisiológico de la célula. En las células hay una constante interconversión entre cisternas y túbulos, y la estructura reticular que forman los túbulos está en constante remodelación. Esto ocurre por ejemplo en células como los hepatocitos, los cuales son capaces de desarrollar metabolismos muy variados dependiendo de las circunstancias, reflejándose en cambios en la organización del retículo endoplasmático. Por otra parte, las cisternas prácticamente desaparecen durante la mitosis y casi todo el retículo endoplasmático aparece en forma de tubos. Sin embargo, la organización global del retículo endoplasmático suele ser más estable en células que están especializadas en una única misión. Así, las células secretoras suelen mantener una gran cantidad de cisternas, mientras que aquellas especializadas en la síntesis de lípidos presentan numerosos túbulos de retículo endoplasmático liso.
Como se han mencionado, las cisternas son más abundantes en las células secretoras (Figura 3), en las cuales se disponen en forma apilada. Al contrario que en el aparato de Golgi, las cisternas contiguas están conectadas por puentes a modo de pliegues de membrana que permiten una continuidad directa entre los espacios internos y las membranas de dichas cisternas. Además del número, cómo se empaquetan las cisternas depende de la actividad secretora, mayor cuanto más secreción. Por ejemplo, en las células de las glándulas salivares, células secretoras, la distancia entre cisternas es de unos 84 nm, mientras que en las neuronas es unos 270 nm. Las cisternas están especializadas en la síntesis y plegamiento de proteínas. Se propone que estos procesos están favorecido en las cisternas respecto a los túbulos por dos características: las cisternas tienen amplias superficies planas de membrana donde se acomodan mejor los ribosomas, en forma de polisomas, hay más translocones y más proteínas relacionadas con la traducción (ver más abajo). Además, la relación volumen/superficie es mayor, por lo que el plegado y control de calidad durante la síntesis de proteínas dispone de más espacio.
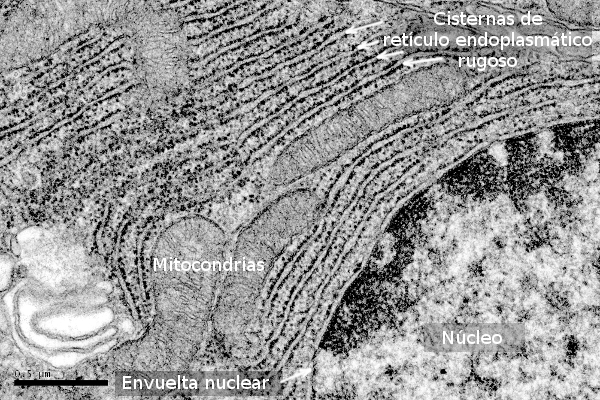
Los túbulos, por su parte, forman una estructura reticular poligonal con una gran capacidad para reorganizarse mediante fusiones o roturas. Independientemente de ello el espesor de una cisterna y el diámetro de un túbulo son similares, de unos 30 nm en levaduras y 50 nm en mamíferos. Curiosamente la separación entre la membrana externa e interna de la envuelta nuclear es también de 50 nm en mamíferos. En el caso de las cisternas, la separación entre las dos membranas se debe a la proteína Climp-63, que se inserta en la membrana y emite hacia el interior de la cisterna un dominio proteico que interacciona con otra Climp-63 localizada en la otra membrana. Estas proteínas tienen un dominio citosólico que interacciona con los microtúbulos. Cuando se aumenta la expresión de esta proteína en una célula hay un aumento de la cantidad de cisternas a expensas de los túbulos. Hay otras proteínas como la RRBP1 que favorecen que las cisternas sean planas. La cantidad de ribosomas asociados a sus membranas condiciona también la forma aplanada, de tal manera que cuando el número de ribosomas asociados aumenta, los túbulos se expanden adoptando la forma de cisternas aplanadas. La densidad de ribosomas puede ser de hasta unos 1000 ribosomas por µm2 en las cisternas, mientras que la densidad es mucho menor cuando aparecen en los túbulos. Aunque los túbulos puedan acomodar ribosomas y la maquinaria de traducción, no son capaces de albergar grandes polisomas o densidades altas de ribosomas asociados.
La organización en túbulos está relacionada sobre todo con la presencia de proteínas llamadas reticulones y la proteína DP1. Ambas tienen una forma de cuña que insertadas en la membrana hace que esta se curve. En humanos hay 7 genes para los reticulones que pueden dar hasta 11 isoformas diferentes. Estas proteínas se insertan en la membrana del retículo a modo de horquillas o cuñas de manera que expanden más la hemicapa citosólica respecto a la luminal (da hacia el interior), lo que produce una curvatura de la membrana. Así, estas proteínas son abundantes en los túbulos y en los bordes de las cisternas. Estas proteínas no crean nuevos túbulos pero sí los estabilizan. Las proteínas reticulón y REEPS (Yop1p en levaduras) convierten a las cisternas en túbulos y su ausencia provoca el cambio contrario. Hay otras proteínas que también influyen en la curvatura de la membrana del retículo como las ARL6IP1, espastina y FAM134. Además, de los dominios que se insertan en las membranas del retículo, todas estas proteínas tienen dominios citosólicos que interaccionan con otros elementos de la célula, como mitocondrias, vesículas, membrana plasmática y con el citoesqueleto.
Los túbulos también incorporan las proteínas GTPasa atlastina, lunapark y las GTPasas Rab 10 y 18, las cuales favorecen la fusión de túbulos y la formación de uniones tripartitas (tres túbulos conectados en un punto). Las atlastinas están relacionadas con las dinaminas y tienen una estructura similar a las mitofusinas, las cuales participan en la fusión mitocondrial. La red general de túbulos se genera y mantiene por el citoesqueleto. Hay otros factores que ayudan en esta plasticidad. Por ejempolo, los ácidos grasos que poseen las membranas del retículo suelen ser más cortos que los de otras membranas de otros compartimentos, y por lo tanto son membranas más delgadas y fluidas que las demás.
2. Síntesis de proteínas
La principal misión del retículo endoplasmático rugoso es la síntesis de proteínas. Esta actividad es muy intensa en aquellas células que tienen por misión la secreción, y es necesaria para cualquier célula. Se estima que una célula promedio sintetiza un tercio de sus proteínas en el retículo endoplasmático. Estas proteínas irán destinadas a diferentes lugares: el exterior celular, el interior de otros orgánulos que participan en la ruta vesicular, como los lisosomas, o formarán parte integral de las membranas, tanto plasmática como las de otros orgánulos de la ruta vesicular. Por ejemplo, todas las proteínas transmembrana de la membrana plasmática se sintetizan en el retículo endoplasmático. Además, el retículo endoplasmático rugoso tiene que sintetizar proteínas para sí mismo, denominadas proteínas residentes. Hay que tener en cuenta que las proteínas sintetizadas en el retículo que van destinadas a orgánulos concretos de la ruta vesicular deben tener unas secuencias de aminoácidos, o modificaciones químicas, que actuarán como señales para que sean reconocidas por los mecanismos de reparto y dirigidas a sus compartimentos diana correspondientes.
Cualquier proteína que se secrete o que forme parte de los orgánulos o compartimentos de la ruta vesicular empieza su proceso de síntesis en ribosomas libres del citosol, pero dicha síntesis terminará en el interior de una cisterna del retículo o formando parte de la membrana de éste (Figura 4). El proceso comienza con la unión de un ARN mensajero (ARNm) a una subunidad pequeña ribosomal y posteriormente a una subunidad grande ribosomal para comenzar la traducción. Lo primero que se traduce de estos ARNm es una secuencia inicial de nucleótidos a partir de la cual se sintetiza una cadena de unos 70 aminoácidos denominada péptido señal. No existe una secuencia común para el péptido señal en todas las proteínas que se han de sintetizar en el retículo endoplasmático, pero cumple tres requisitos: unos 30 aminoácidos hidrofóbicos, una corta cola polar y una secuencia corta básica. Una molécula conocida como SRP (sequence recognizing particule), que es una mezcla de 1 molécula de ARN y 6 polipéptidos, reconoce al péptido señal y enlentece el proceso de traducción. SRP tiene una estructura molecular con una cavidad formada por aminoácidos metionina donde encaja la secuencia hidrofóbica del péptido señal. Una vez reconocida la secuencia señal la propia molécula SRP interactúa con el ribosoma y bloquea la zona donde se une el factor de elongación, necesario para que la traducción continúe. Por tanto la unión de SRP a la secuencia señal detiene la traducción. Estas modificaciones de la estructura del SRP hace que exponga hacia el exterior una secuencia de aminoácidos que serán reconocidos posteriormente por el receptor de SRP, localizado en las membranas del retículo endoplasmático.

El complejo formado por ribosoma, ARNm, péptido señal más SRP difunde por el citosol hasta chocar con una membrana del retículo endoplasmático, a la cual se une gracias a la existencia de un receptor de membrana que reconoce al SRP. Todo el conjunto anterior interacciona con un translocador, que es complejo formado por tres proteínas transmembrana que forma un canal por el cual penetra la cadena polipeptídica naciente hacia el interior de la cisterna del retículo endoplasmático. El translocador suele estar asociado a moléculas como enzimas y otras proteínas, y al conjunto se le denomina translocón. El translocador tiene la capacidad de cerrarse cuando no está asociado a un proceso de traducción. Esto es interesante porque evita el trasiego de iones a su través, sobre todo el calcio, puesto que el retículo es un almacén de calcio celular. El péptido señal queda unido al translocador mientras que el resto de la cadena polipeptídica se va traduciendo y liberando hacia el interior. Una peptidasa presente en el retículo escinde el péptido señal del resto de la cadena de aminoácidos, quedando ésta libre en el interior. Una vez completada la síntesis, la cadena de aminoácidos adopta su conformación tridimensional, ayudada por chaperonas, y el ribosoma y el ARNm se liberan de la membrana del retículo, listos para otro ronda de tranducción.
Si la proteína que se está sintetizando es una proteína transmembrana no será entonces liberada al interior del retículo. La cadena polipeptídica naciente tiene secuencias de aminoácidos hidrófobos que cuando se traducen facilitan su inserción directamente entre los ácidos grasos de la membrana gracias a la acción del translocador. El translocador es capaz de abrirse por uno de sus lados y poner en contacto el interior del canal con las cadenas de ácidos grasos. El proceso es muy complejo y diverso para los diferentes tipos de proteínas integrales puesto que, por ejemplo, algunos receptores transmembrana tiene hasta siete cruces de membrana donde se alternan secuencias que han de insertarse en la membrana con otras que quedan bien en el lado citosólico o bien en el interior de la cisterna del retículo endoplasmático. Sólo en raras ocasiones el retículo importa proteínas que se sintetizan completamente en el citosol gracias a ciertos transportadores presentes en su membrana.
Es interesante mencionar que las membranas del retículo facilitan esta actividad sintetizadora ya que son más delgadas (unos 5 nm) y más fluidas que otras membranas, por lo que la inserción y plegamiento de proteínas transmembrana es más fácil. Por ejemplo, tienen una gran concentración de glicerofosfolípidos con baja tasa de saturación (menos del 15 %), además de tener una carga neta neutras en la cara citosólica.
Otro aspecto interesante es que las proteínas son modificadas conforme van siendo sintetizadas. a) Hay glicosilación (N-glicosilación) de los aminoácidos asparragina. Éstos recibirán un complejo de 14 azúcares en su radical, que son transferidos desde un lípido embebido en la membrana denominado dolicol fosfato, perdiéndose algunos de estos azúcares en procesos posteriores. b) Se da hidroxilación en algunas proteínas, sobre todo en aquellas que van a formar parte de la matriz extracelular. Aquí se hidroxilan los aminoácidos prolina y lisina, dando hidroxiprolina e hidroxilisina, que formarán parte del colágeno. c) Se establecen puentes disulfuro en aquellas proteínas formadas por dos cadenas polipeptídicas. d) Algunas proteínas asociadas a la membrana plasmática están unidas químicamente a lípidos de la membrana, y estos enlaces también se producen en el retículo endoplasmático.
Control de calidad. Sistema ERAD.
Por diversas causas se pueden producir fallos en el plegamiento de las proteínas que se están sintetizando en el retículo endoplasmático, pudiendo dar lugar a moléculas peligrosas para la célula. El mal plegamiento de proteínas es más frecuente de lo que podría parecer. Curiosamente, el plegamiento de las proteínas es el punto más propenso a errores en toda la cadena de expresión génica desde la transcripción hasta tener la proteína funcional. Por ejemplo, en el caso de la proteína CFRT (regulador transmembrana de la fibrosis quística) es de un 80 %.
En el retículo endoplasmático se produce un control de la calidad de las proteínas sintetizadas, de modo que aquellas que tienen defectos, normalmente por un mal plegamiento, son sacadas al citosol y eliminadas, y se permite pasar a la vía secretora sólo a aquellas proteínas que están correctamente plegadas. Este sistema de vigilancia lo forman las chaperonas, proteínas que detectan los errores de plegamiento y marcan a las proteínas defectuosas para su degradación. Otras proteínas con dominios tipo lectina, reconocen determinados azúcares y comprueban la adición correcta de glúcidos. La degradación de las proteínas malformadas se produce mediante un proceso denominado ERAD (ER associated degradation).
La secuencia del funcionamiento del sistema ERAD para proteínas solubles en el interior del retículo se inicia con un reconocimiento de las proteínas mal plegadas, translocación a través de la membrana del retículo, ubiquitinación en el lado citosólico, modificación por una AAA-ATPasa y degradación por proteosomas (Figura 5). Para las moléculas transmembrana el proceso es similar, pero pueden ubiquitinarse en su dominio citosólico primero y después ser sacadas de la membrana hacia el citosol. El sistema ERAD es en realidad un sistema complejo de vías moleculares que funcionan en paralelo pero que básicamente realizan estos pasos.

El sistema ERAD tiene también otras funciones como el control de la homeostasis de lípidos, mantenimientos de la identidad del retículo, organización de la envuelta nuclear, media en el contacto entre orgánulos, flujo de calcio, señalización del sistema inmune innato.
Cuando las proteínas mal plegadas se producen en exceso, y el sistema ERAD no es capaz de eliminarlas, estas proteínas se acumulan en el retículo. Hay muchas causas por las que se puede producir un aumento de fallos en el plegamiento proteico y su acumulación: aumento de la síntesis de proteínas, fallo en la vía de degradación proteica de la ubiquitina-proteosoma, autofagia deficiente, escasez de energía, exceso o limitación de nutrientes, desregulación de los niveles de calcio, fallo de la homeostasis de los procesos de oxidación-reducción, hipoxia, etcétera. La acumulación de proteínas defectuosas conlleva el inicio de mecanismos moleculares para recuperar la proteostasis (homeostasis de proteínas) de manera que la célula pueda seguir viviendo, o, si el estrés es crónico o muy severo, iniciar la muerte celular por apoptosis. A estos mecanismos moleculares se les llama en conjunto UPR (unfolded protein response). Consisten en la síntesis de chaperonas específicas para reducir el número de proteínas mal plegadas y en una ralentización de la síntesis de proteínas en general, además de incrementar los procesos de degradación proteica. El mecanismo UPR puede venir acompañado por un aumento de la degradación del propio retículo mediante autofagia.
En las enfermedades neurodegenerativas como el Alzheimer y el Parkinson hay mutaciones que producen acumulación de proteínas mal plegadas, como la beta-amiloide y la alfa-sinucleina, respectivamente. La vía UPR es un elemento que inicialmente intenta prevenir este estrés celular por malformación proteica, pero, como la acumulación de proteínas es muy intensa y no puede recuperar la homeostasis, colabora en el inicio de la vía apoptótica y muerte celular. El estrés del retículo también parece ser relevante en ciertas enfermedades metabólicas relacionadas con la regulación de la glucosa y los lípidos, y en el cáncer.
En las plantas, las síntesis de proteínas puede ser para usarlas como almacén de energía. Estas proteínas son trasladadas a las vacuolas, o en algunas especies, ser almacenadas en el propio retículo endoplásmatico.
3. Síntesis de lípidos
En las membranas del retículo endoplasmático liso se producen la mayoría de los lípidos requeridos para la elaboración de las nuevas membranas de la célula, incluyendo glicerofosfolípidos y colesterol. Además, aunque gran parte de la síntesis de los esfingolípidos se lleva a cabo en el aparato de Golgi, su estructura básica, la ceramida, se sintetiza también en el retículo endoplasmático. Sin embargo, en las membranas del retículo no se realizan todos los pasos de la síntesis de los lípidos de las membranas, y es más una plataforma de ensamblado que de síntesis desde cero. Los ácidos grasos se sintetizan en el citosol y son insertados posteriormente en las membranas del retículo endoplasmático liso donde son transformados en glicerofosfolípidos. Este ensamblado lo realizan proteínas de membrana que tienen sus centros activos orientados hacia el citosol y por tanto los lípidos estarán inicialmente en la hemicapa citosólica de la membrana. Como el cambio pasivo de los lípidos entre hemicapas, o movimiento "flip-flop", es difícil por el ambiente hidrófobo de las cadenas de ácidos grasos de la membrana, para que algunos de ellos lleguen a la hemicapa interna desde la citosólica se requiere la existencia de proteínas transportadoras de lípidos, denominados flopasas y "mezcladoras" (scramblases en inglés). Aunque las membranas del retículo endoplasmático tienen más fosfatidil serina y poco fosfatidilinositol en la hemicapa interna, las dos hemicapas son muy parecidas en cuanto a composición, por lo que se dice que son simétricas. Así, la asimetría que se encuentra en las membranas de otros orgánulos se debe a la presencia diferencial de estas enzimas translocadoras, además de otras denominadas flipasas, pero también a procesos metabólicos que eliminan o cambian unas especies de lípidos por otras. Por tanto, en cuestión de lípidos, la localización asimétrica de éstos en las membranas no depende de la síntesis inicial en el retículo endoplasmático.
El colesterol es otro importante componente de las membranas, sobre todo de la plasmática, que se sintetiza mayoritariamente en el retículo endoplasmático liso. Desde aquí es transportado por la vía vesicular o por transportadores proteicos solubles. Por ejemplo, las levaduras, que poseen ergosterol en sus membranas en vez de colesterol, usan vías no vesiculares para transportar el ergosterol desde el retículo hasta la membrana plasmática. Estos transportadores son diversos y sus movimientos son independientes de ATP.
Por la vía vesicular, formando parte de vesículas, los lípidos sintetizados en el retículo endoplasmático liso se reparten a las membranas de otros orgánulos (Figura 6). Sin embargo, las mitocondrias y los peroxisomas no forman parte de la ruta vesicular por lo que muchos de sus lípidos de membrana deben ser importados desde el retículo endoplasmático por otros mecanismos. Por ejemplo, para los glicerofosfolípidos existen unas proteínas solubles llamadas intercambiadoras de glicerofosfolípidos que tienen la habilidad de transportarlos a través del citosol. Estos transportadores toman en la membrana del retículo endoplasmático liso y los sueltan en las de estos orgánulos. Otro mecanismo de intercambiar lípidos entre membranas de orgánulos que no están en la ruta vesicular es por contacto directo entre sus membranas. Se ha observado con el microscopio electrónico que en algunos puntos las membranas del retículo están muy próximas a las de las mitocondrias y a los peroxisomas, lo que parece indicar que el retículo procura lípidos a estos orgánulos directamente de membrana a membrana, mediado por por un transportador. Los peroxisomas se forman inicialmente a partir de cisternas del retículo. Las mitocondrias y los cloroplastos pueden sintetizar parte de los lípidos de sus membranas. Así, los cloroplastos sintetizan sus propios glicerofosfolípidos y glicolípidos, aunque también se observan contactos directos de los cloroplastos con las membranas del retículo endoplasmático.

En el retículo endoplasmático liso también se sintetizan lípidos como los triacilgliceroles que serán almacenados en el propio retículo o en gotas lipídicas citosólicas. Este proceso es muy activo en los adipocitos, los cuales contienen una gran cantidad de retículo endoplasmático liso Los adipocitos sintetizan y almacenan grasa con dos funciones: reserva alimenticia y aislamiento térmico. También es el principal responsable de la síntesis de la parte lipídica de las lipoproteínas, de la producción de hormonas esteroideas y de ácidos biliares. Por ejemplo, las células de Leydig en los testículos sintetizan hormonas esteroides y tienen por ello un retículo endoplasmático liso muy desarrollado.
4. Detoxificación
Los hepatocitos, las células típicas del hígado, tienen un retículo endoplasmático liso muy desarrollado. En él se sintetizan las lipoproteínas que transportarán al colesterol y a otros lípidos al resto del organismo. En sus membranas se encuentran también enzimas, como la familia de proteínas P450, responsables de la eliminación de productos del metabolismo potencialmente tóxicos, así como algunas toxinas liposolubles incorporadas durante la ingesta. La superficie de membrana del retículo se adapta a la cantidad de enzimas detoxificadoras sintetizadas, la cual depende a su vez de la cantidad de tóxicos presentes en el organismo. La forma de los túbulos y la carencia de ribosomas en sus membranas tendrían la ventaja de ofrecer más superficie de membrana respecto al volumen del orgánulo.
5. Homeostasis de glucosa
La glucosa se suele almacenar en forma de glucógeno, fundamentalmente en el hígado. Este órgano es el principal encargado de aportar glucosa a la sangre, gracias a la regulación llevada a cabo por las hormonas glucagón e insulina. La degradación del glucógeno produce glucosa-6-fosfato que no puede atravesar las membranas y por tanto no puede abandonar las células. La glucosa 6-fosfatasa, que está anclada a las membranas del retículo endoplasmático, se encarga de eliminar ese residuo fosfato, permitiendo que la glucosa sea transportada al exterior celular.
6. Almacén de calcio
El retículo endoplasmático está también especializado en el secuestro y almacenaje de calcio procedente del citosol, gracias a bombas de calcio localizadas en sus membranas. La concentración de calcio en el interior del retículo es del orden de milimolar (mM), mientras que en el citosol es de nanomolar (nM). Este calcio puede salir de forma masiva en respuesta a señales extra o intracelulares gracias a cascadas de segundos mensajeros, y desencadenar respuestas de las células como la exocitosis. Otro ejemplo destacable es el retículo sarcoplasmático (nombre que recibe el retículo endoplasmático liso en las células musculares) que secuestra calcio gracias a una bomba de calcio presente en sus membranas. El secuestro y la salida de calcio desde el retículo sarcoplasmático se produce en cada ciclo de contracción de la célula muscular.
7. Formación de vesículas
Ir a esta página.
8. Contactos entre membranas
Ir a esta página.
Las cisternas y túbulos del retículo endoplasmático se observan en estrecha aposición a otras membranas de la célula cuando se observan imágenes tomadas con el microscopio electrónico. Entre las membranas con las que contactan están las de las mitocondrias, endosomas, aparato de Golgi, gotas de lípidos y membrana celular.
Retículo-membrana plasmática. En levaduras, del 20 al 40 % de la membrana plasmática está recubierta por el retículo endoplasmático. Se ha comprobado que al menos 6 proteínas participan en mantener esta proximidad, y algunas de estas proteínas tienen la propiedad de transferir lípidos, por lo que esta unión podría tener como función el intercambio de lípidos entre ambos compartimentos. Los contactos entre el retículo y la membrana plasmática son también evidentes en las células musculares, donde la transmisión de un gradiente electroquímico parece su principal función.
Retículo-mitocondria. Los contactos entre las membranas del retículo y la membrana externa de la mitocondria se observan con frecuencia. El papel de estos contactos parecen estar relacionados con la regulación de la concentración de calcio, puesto que ambos orgánulos son almacenes intracelulares de calcio, y la transferencia de lípidos entre ambas membranas, sobre todo de fosfolípidos desde el retículo hasta la mitocondria. Pero también parecen estar implicados en los procesos de fisión de mitocodrias puesto que reclutarían moléculas para que la división de la mitocondria se produjera. Estos contactos son realmente anillos de retículo endoplasmático que envuelven a la mitocondria. El lugar de este anillo es el lugar donde se produce la división de la mitocondria. Recientemente también se señalan estos contactos como elementos que participan en la formación del autofagosoma.
Retículo-Golgi. Cisternas del retículo endoplasmático se ven frecuentemente en contacto con las membranas trans del aparato de Golgi, donde se cree que hay un trasvase de ceramidas y estéroles desde el retículo hasta el aparato de Golgi. Las ceramidas son esenciales para la síntesis de los esfingolípidos, lo cual ocurre en el aparato de Golgi.
Retículo-endosomas. Los contactos entre el retículo y los endosomas parecen regular aspectos de la vida de los endosomas tales como su división (reclutan proteínas para la fisión), maduración y movimiento (modifican moléculas que interaccionan con el citoesqueleto). Al igual que en el caso de las mitocondrias se han observado anillos de túbulos de retículo alredor de los endosomas, los cuales participarían de alguna manera en la división del endosoma. Además, se propone que hay una transferencia de colesterol desde los endosomas hasta el retículo.
9. Formación de peroxisomas.
Ir a esta página.
10. Formación de gotas de lípidos.
Ir a esta página.
11. Autofagia
Ir a esta página.
-
Bibliografía ↷
-
Bibliografía
Arruda AP, Parlakgül G. 2022. Endoplasmic reticulum architecture and inter-organelle communication in metabolic health and disease. Cold spring harbor perspectives in biology. 15(2):a041261. doi: 10.1101/cshperspect.a041261.
Christianson JC, Carravalho P. 2022. Order through destruction: how ER-associated protein degradation contributes to organelle homeostasis. The EMBO journal. 41: e109435. DOI 10.15252/embj.2021109845.
English AR, Zurek N, Voeltz GK. 2009. Peripheral ER structure and function. Current opinion in cell biology. 21:506-602.
Daleke DL. 2007. Phospholipid Flippases. The journal of biological chemistry. 282:821-825.
Nixon-Abell J, Obara, CJ, Weig VA, Li D, Legant WR, Xu CS, Pasolli HA, Harvey K, Hess HF , Betzig E, Blackstone C, Lippincott-Schwartz3 J. 2016. Increased spatiotemporal resolution reveals highly dynamic dense tubular matrices in the peripheral ER. Science. 354: 3928-2.
-
 Tráfico vesicular
Tráfico vesicular 